Foundationelektroforese, teknikk, hva er det for, eksempler

- 4117
- 976
- Daniel Skuterud
De Elektroforese Det er en teknikk som brukes til å skille molekyler i et elektrisk felt. Det må gjøre, spesifikt, med migrasjonen av partikler lastet under påvirkning av en elektrisk strøm påført mellom to stolper, en positiv og en annen negativ.
Elektroforese er for tiden en av de mest rutinemessige prosedyrene som foregår under utviklingen av et eksperiment, spesielt innen felt relatert til analytisk kjemi, biokjemi og biologisk og medisinsk vitenskap generelt.
 Elektroforesebøtte. Kilde: Melodygar/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0)
Elektroforesebøtte. Kilde: Melodygar/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0) Det brukes til å skille protein, peptider, DNA, RNA og andre i henhold til deres belastning, størrelse, tetthet og renhet.
De forskjellige kommersielle husene har designet forskjellige formater, med forskjellige applikasjoner og passende fortjeneste for spesifikke formål, men alle prosedyrer krever de samme grunnleggende elementene:
- En energikilde for å generere elektrisk lading
- Et støtte for separasjon
- En bufferløsning (buffer) For å holde pH konstant
[TOC]
Basis
Elektroforese er ikke annet enn migrasjonen (separasjonen) av partikler eller belastede molekyler (naturlig eller kunstig) i et medium eller støtte under påvirkning av et elektrisk felt.
Teknikken er basert på en av de viktigste fysiske ligningene av elektromagnetisme, hvor styrken er lik den elektriske ladningen multiplisert med det elektriske feltet som brukes på det punktet (F (kraft) = Q (elektrisk ladning) x E (elektrisk felt ).
I henhold til denne ligningen vil to partikler med samme masse, men med forskjellig belastning, bevege seg til forskjellige hastigheter i samme elektriske felt. I tillegg vil bevegelseshastigheten til disse partiklene avhenge av forholdet mellom belastningen og massen.
Forskere har benyttet seg av disse egenskapene og last/masseforhold for å skille komponentene fra biomolekyler i sine minste deler, samt for å skille forskjellige molekyler i en blanding, blant andre applikasjoner.
Det er viktig å huske at biologiske molekyler som aminosyrer, peptider, proteiner, noen karbohydrater, nukleotider og nukleinsyrer alle har noe vi kaller "ioniserbare grupper", slik at de kan eksistere som positive eller negativt ladede arter under visse betingelser i pH.
Teknikk
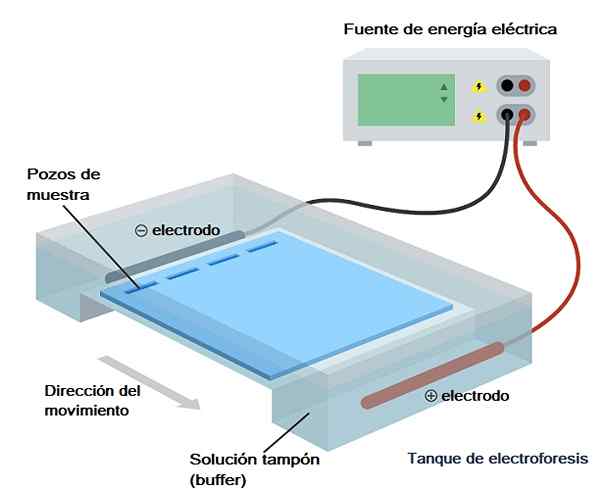
Selv om det er forskjellige typer elektroforese, er gelelektroforese den mest brukte i biokjemisk analyse, molekylærbiologi og bioteknologi, så det vil være det vi vil snakke om kort i tekniske termer.
Som navnet tilsier, innebærer gelelektroforese bruken av et fast, formet faststøttemedium, enten for analyse/separasjon av blandinger av protein eller nukleinsyrer (DNA og/eller RNA) under påvirkning av et elektrisk felt.
Systemet eller apparatet som brukes til å utføre en elektroforetisk "kjøring" kan være horisontalt (vanligvis brukt til nukleinsyrer) eller vertikal (vanligvis brukt til protein).
- Eksempel på nukleinsyreelektroforeseteknikken
Nukleinsyrer skilles vanligvis ved bruk av agarosegeler (galaktosepolysakkarid) som fremstilles med en tilstrekkelig bufferoppløsning (Tris/acetat/EDTA eller Tris/Borato/EDTA) og hvis konsentrasjon vil bestemme "oppløsningen" av fragmenter i forskjellige størrelser.
Kan tjene deg: Jordens næringskjede: lenker og eksempelPrøveforberedelse
Det første trinnet før du utfører et elektroforetisk løp i en agarosegel er å oppnå prøven. Dette vil avhenge av den eksperimentelle enden, og prøvene kan være et produkt av en enzymatisk fordøyelse, på en polymerasekjedereaksjon (PCR), en rensing av nukleinsyrer, etc.
 Blanding av prøven med lastbuffen.Org/lisenser/av/4.0) via Wikimedia Commons)
Blanding av prøven med lastbuffen.Org/lisenser/av/4.0) via Wikimedia Commons) Etter å ha oppnådd, blandes dette med en farget løsning (belastningsløsning) som tillater rask avsetning av prøven i en brønn, siden den har glyserol og et fargestoff som tillater kjøringen visuelt.
Gelforberedelse
Dette trinnet består i å blande den nødvendige mengden av geleringssubstratet (agarosen) med bufferløsningen, smelte det ved hjelp av varme og stivne det på en støtte som fungerer som "mugg".
Under gelifiseringen blir noen "kammer" introdusert i gelen plassert i "formen" for å avgrense "brønnene" der prøvene vil bli introdusert før kjøringen.
Når gelen er avkjølt og størknet, blir "kamene" fjernet og den blir introdusert i en beholder kjent som "bøtte", som er full av løpende bufferløsning, (Tris/acetat/EDTA eller Tris/Borato/Borato/EDTA).
Denne bøtta er på sin side inkludert i det som kalles "elektroforetisk kammer", som ikke er noe mer enn beholderen som det elektriske feltet føres og som har et rom der gelen blir introdusert og to seksjoner som de er fylt med bufferløsning (buffer løpe).
Dette kameraet har to elektroder, en positiv og ett negativt, hvorav ionebevegelsen produseres etter påføring av et elektrisk felt (det er koblet til en strømkilde).
Laster prøver
Når prøvene har blandet seg med den respektive belastningsløsningen, blir disse introdusert i "brønnene" som tidligere er laget i gelen.
Siden nukleinsyrer har en negativ nettbelastning, vandrer de fra den negative polen til det positive, så dette må tas i betraktning når kameraet er koblet til strømkilden, noe som sikrer at den negative polen tilsvarer det mest stedet ved siden av stedet der prøvene ble lastet.
Corrida Time er etablert i streng avhengighet av forskeren som er ansvarlig for eksperimentet. Spenningen beregnes vanligvis i et 5 volt -forhold per centimeter i gelen som skiller de to elektrodene.
Vise
Når gelen går (når prøvene har reist gelen fra den ene enden til den andre), er den nedsenket i en løsning av etidbromid (ETBR), et fargestoff som er ispedd mellom nitrogenholdige baser og at "merket", så så De kan visualiseres i en transilumenant ved bruk av ultrafiolett lys.
Hva er elektroforese for?
Elektroforese har historisk blitt brukt med flere formål. I dag avhenger imidlertid nytten i stor grad av "spørsmålet" som forskeren blir stilt i forhold til et fenomen eller et bestemt system, samt typen elektroforese som han ønsker å bruke.
Kan tjene deg: topoisomerase: hva er, egenskaper, funksjoner, typerVi kan imidlertid for å verve noen av hovedfunksjonene som denne teknikken har, og starter med de mest "sjeldne" og slutter med de mest populære og for det meste utnyttet i biologiske vitenskapsverden. Elektroforese er nyttig:
- For den kvantitative analysen av komplekse blandinger av makromolekyler og for beregning av den potensielle "zeta" (kolloidal egenskap til en partikkel i et flytende medium under påvirkning av et statisk elektrisk felt).
- For analyse av blodsera for diagnostiske formål.
- For separasjon av glukoproteiner, lipoproteiner og blodhemoglobin.
- For matanalyse, farmasøytiske produkter og miljøgifter.
Elektroforese i agarosegeler
- For separasjon av DNA -fragmenter etter fordøyelse med begrensningsenzymer.
- For separasjon av nukleinsyremolekyler før overføring til membraner for påfølgende analyser.
- For analyse av PCR -produkter (polymerasekjedereaksjon) som verifiserer om det skjedde eller ikke.
- For estimering av størrelsen på molekylene i en blanding av DNA eller RNA.
- For estimering av mengden og/eller kvaliteten på rensede nukleinsyrer.
Elektroforese i polyakrylamidgeler under denaturalisering eller naturlige forhold
- For å bestemme størrelsen på et protein.
- Å identifisere proteiner.
- For å bestemme renheten til en prøve etter flere rensetrinn.
- For å identifisere tilstedeværelsen av intramolekylære disulfidkoblinger.
- For å bestemme interaksjonen mellom proteiner.
- For å bestemme det isoelektriske punktet til et protein.
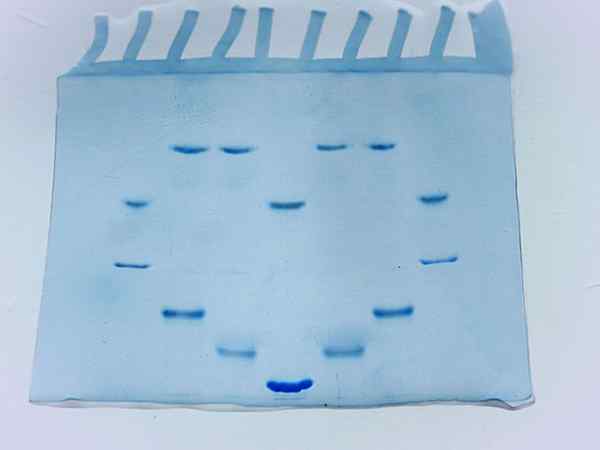 Fotografering av en akrylamidgel etter kjøringen av flere proteinprøver (kilde: Larionova.Marina/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0) via Wikimedia Commons)
Fotografering av en akrylamidgel etter kjøringen av flere proteinprøver (kilde: Larionova.Marina/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0) via Wikimedia Commons) Faktorer som påvirker elektroforese
Migrasjonen av en partikkel i et elektrisk felt avhenger av forskjellige faktorer, blant dem er:
- Din elektriske lading
- Dens molekylære størrelse
- Dens hydrofobisitet og dens form
- Størrelsen på det elektriske feltet som påføres
- Systemtemperatur og ionisk kraft av bufferløsningen som brukes
- Miljøets natur der det ligger
I forhold til prøven
Blant parametrene relatert til partikler (prøve) som er underlagt et elektrisk felt, har hovedfaktorene som påvirker denne prosessen å gjøre med belastningen, deres størrelse og form.
Jo større nettlas. Forholdet til størrelse er imidlertid omvendt proporsjonalt, noe som betyr at jo mer "stor" molekylet, desto saktere migrerer.
Det kan tjene deg: Lia Agar (Iron Lysine): Hva er, grunnlag, forberedelse, brukerI forhold til det elektriske feltet
Så langt har vi snakket om viktigheten av det elektriske feltet for å oppnå bevegelse av en partikkel ved elektroforese, men vi har ikke definert hva det er: elektrisk kraft per lastenhet eller, på enklere vilkår, et område med rom der det er en elektrisk kraft.
Parametrene angående det elektriske feltet som kan påvirke migrasjonen er spenning, strøm og motstand.
Spenningen påvirker "flytid" til molekylene som er atskilt etter påføring av det elektriske feltet. Jo høyere det er, jo raskere beveger disse seg.
Strømmen (kontinuerlige og ensartede elektroner som "skyves" av spenningskilden) er utført mellom elektroforetiske systemelektroder takket være ionene som er til stede i bufferløsningen. Er direkte relatert til spenning.
I forhold til bufferløsningen
Sammensetningen, ionisk kraft og pH i bufferløsningen er hovedparametrene som påvirker et elektroforetisk "kjøring", da de direkte påvirker noen av egenskapene til prøvene, spesielt den elektriske ladningen.
Fordi? Bufferløsningen stabiliserer pH i støttemediet der elektroforese oppstår. Sammensetningen kan påvirke forskyvningen av vandrende partikler og den ioniske konsentrasjonen også, da den er direkte relatert til strømmen.
I forhold til støttemediet
De forskjellige typene og formatene for elektroforese presenterer også forskjellige medier som migrasjon skjer og hvor den senere kan "registreres".
Migrasjonshastigheten til molekylene utsatt for elektroforese avhenger av typen støttemedium, som vanligvis skal være inert.
Dens absorpsjonsegenskaper, elektroendo-osmose er viktig (bevegelseskapasitet for en væske gjennom en membran under påvirkning av et elektrisk felt) og dets molekylære silekapasitet.
Eksempler på bruk av elektroforese
Klassiske eksempler på elektroforetiske teknikker brukt i biologi og bioteknologi inkluderer:
- Elektroforese i agarosegeler (engelsk Elektroforesegel)
- Elektroforese i akrylamidgeler under denaturaliserende forhold (SDS-PAGE, engelsk Natriumdodecylsulfat polyakrylamidgelelektroforese)
- Elektroforese i akrylamidgeler under innfødte forhold (BN-side, engelsk Blå naturlig polyakrylamidgelelektroforese)
- Elektroforese i to dimensjoner (2D-side, fra engelsk Todimensjonal polyakrylamidgelelektroforese)
- Kapillærelektroforese (fra engelsk Elektroforese kapillær)
- Isolektroenfoque (engelsk Isolektrofokosing)
- Pulsert feltelektroforese (engelsk Pulsert feltelektroforese)
Referanser
- Beck, Kevin. (2020, 25. mai). Typene elektroforese. Scienting.com. Hentet fra vitenskap.com
- Essays, Storbritannia. (November 2018). Elektroforesetyper og applikasjoner. Hentet fra ukessays.com
- Nelson, d. L., Lehninger, a. L., & Cox, m. M. (2008). Lehninger prinsipper for biokjemi. Macmillan.
- Parmar, p. (August 2018). Elektroforese: Betydning, definisjon og klassifisering (med diagram). BIO -teknologi. Hentet fra bioteknologi.com
- Perrett, d. (2010). 200 års elektroforese. Kromatog. I dag, 4-7.
- Righetti, p. G. (2005). Elektroforese: March of Pennies, March of Dimes. Journal of Chromatography A, 1079 (1-2), 24-40.
- Rilbe, h. (nitten nitti fem). Noen minner om elektroforesens historie. Elektroforese, 16 (1), 1354-1359.
- Vesterberg, eller. (1993). En kort historie med elektroforetiske metoder. Elektroforese, 14 (1), 1243-1249.
- Vinayagam, m. (Ingen dato). Faktorer som påvirker elektroforese. Akademi.Edu. Hentet fra akademia.Edu
- « Kjemisk balanseforklaring, faktorer, typer, eksempler
- TOLTEC KULTUR Origin, beliggenhet, egenskaper, organisering »

