Aromatiske hydrokarbonegenskaper, eksempler, applikasjoner
- 3679
- 412
- Anders Mathisen
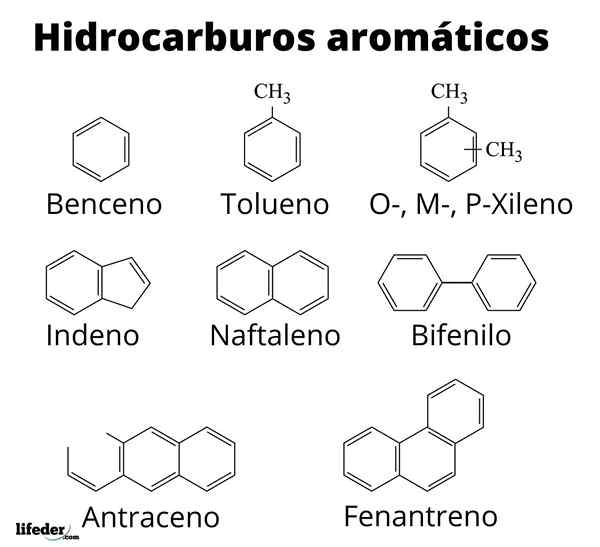
De aromatiske eller sandhydrokarboner De er et sett med organiske forbindelser som bare er sammensatt av karbonatomer og hydrogener, og som er preget av å ha enheter av benzenringer i sine molekylære strukturer.
Noen, som navnet hans understreker, skyter søte og behagelige lukt; grunn til at de første organiske kjemikaliene omtalte dem som aromatiske. Metangass er for eksempel et toaletthydrokarbon; Mens toluen, flyktig væske, presenterer en ganske særegen og sterk lukt.
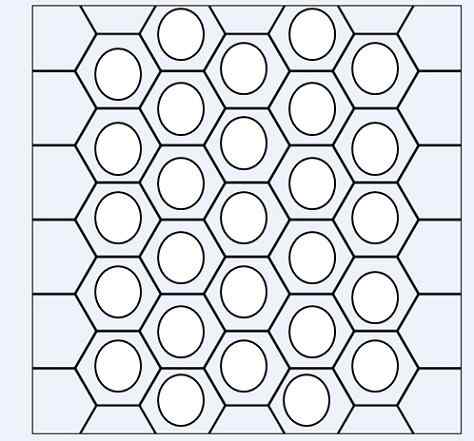 Aromatiske hydrokarboner gjenkjennes av Benncytenic Rings -enheter
Aromatiske hydrokarboner gjenkjennes av Benncytenic Rings -enheter I det øvre bildet har vi et slags nettverk eller nett sammensatt av Benzenic Rings. Legg merke til dine sekskantede geometrier og sirkelen inni. Denne sirkelen representerer det som er kjent som aromatisitet, som er en helt kjemisk og ikke -fysisk egenskap, uavhengig av lukten av disse hydrokarbonene.
Aromatiske hydrokarboner er blant de viktigste, ekstraherte eller produserte, olje- og karbonmineraler. Benzen er hjørnesteinen i disse hydrokarbonene og deres anvendelser, siden fra den stammer symfiner av forbindelser som brukes som råstoff til produksjon av gjødsel, plast, lim, vaskemidler, parfymer, medisiner, etc.
[TOC]
Hvordan heter aromatiske hydrokarboner?
En enkelt benzenring
For aromatiske hydrokarboner har vi den særegne at deres tradisjonelle, eller vanlige navn vanligvis råder over de som styres av IUPAC -nomenklaturen.
Alle inneholder benzenringen, eller en ring som oppfyller aromatisk egenskap. De enkleste kan navngis i henhold til benzen og de relative stillingene til deres substituenter.
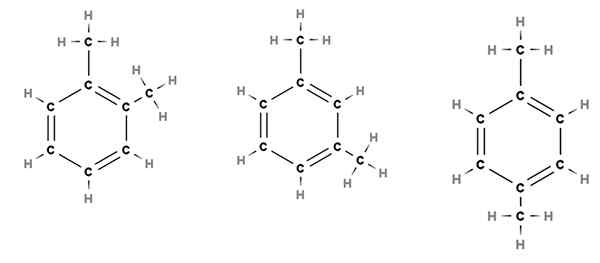 Relative posisjoner av substituentene i en benzenisk ring for dimetylbenzenmolekylet. Kilde: Gabriel Bolívar via Molview.
Relative posisjoner av substituentene i en benzenisk ring for dimetylbenzenmolekylet. Kilde: Gabriel Bolívar via Molview. Tenk for eksempel på det øvre bildet. I de tre strukturene ser vi den sekskantede ringen til benzen, som har to metylsubstituenter, Cho3. Dermed kalles denne forbindelsen dimetylbenzen, fordi den består av en benzen med to metylos.
Kan tjene deg: Kaliumsulfat (K2SO4): Struktur, egenskaper, bruksområder, synteseFra venstre mot høyre ser vi at skillet mellom de to3 Det blir større, som ikke bare påvirker molekylets fysiske egenskaper, men også endrer deres respektive navn. For å differensiere dem, siden de alle kalles dimetylbenzen, brukes orto prefikser (o-), mål (m-) og for (p-) brukes (p-).
Derfor, og igjen, fra venstre mot høyre har vi: orto-dimetylbenzen, meta-dimetylbenzen og parameterbenzen. Imidlertid er det tradisjonelle navnet på denne forbindelsen xylenet, så navn blir: orto-xylen, meta-xylen og para-xylen.
Hvis det er mer enn to forskjellige substituenter, brukes det til å oppregne karbonatomer etter de samme nomenklaturreglene som for alle hydrokarboner.
Flere ringer
For aromatiske hydrokarboner med mer enn en benzenisk ring blir tradisjonelle navn enda viktigere. Dette er fordi de systematiske navnene som beskriver strukturene deres er tungvint og vanskelige å huske. Tenk på eksemplet på naftalen:
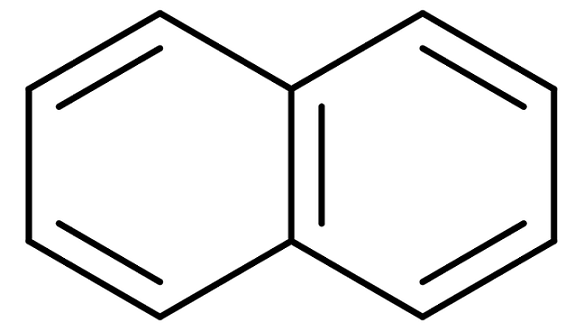 Naftalenstruktur
Naftalenstruktur Naftalen er også kommersielt kjent som naftalin eller hvit kamfer. Imidlertid er det systematiske navnet: Biciclo [4,4,0] des-1,3,5,7,9 pentan. Og dette bare for en forbindelse med to sammenslåtte benzeniske ringer; Nomenklaturen blir mye mer komplisert for forbindelser med tre eller flere ringer.
Egenskaper til aromatiske hydrokarboner
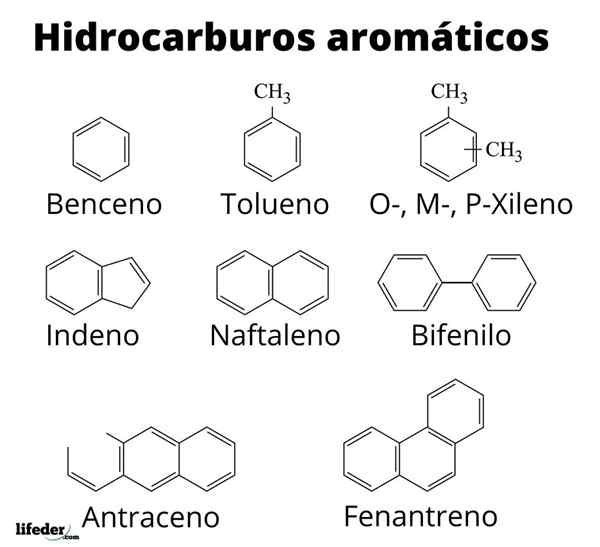 Struktur av noen aromatiske hydrokarboner
Struktur av noen aromatiske hydrokarboner Aromatisitet
Aromatiske hydrokarboner inneholder ringer som overholder Huckel -regler. Det vil si at ringene deres må ha atomer med SP -hybridiseringer2, Vær så flat som mulig, og ha et antall elokkerte π -elektroner lik 4n + 2. For eksempel er benzen aromatisk fordi den har 6 demokerte elektroner for n= 1 (4 · 1 + 2 = 6).
Høye C/H -forhold
C/H -forhold for aromatiske hydrokarboner er høye eller større enn 1. For eksempel for benzen, c6H6, C/H er lik 6/6 eller 1. I mellomtiden, for naftalen, C10H8, C/H er lik 10/8 eller 1.25. Hva betyr dette? At disse hydrokarbonene er veldig "kullsyreholdige" sammenlignet med andre forbindelser.
Kan tjene deg: sulfonsyre: struktur, nomenklatur, egenskaper, brukGule flammer
Nettopp på grunn av deres høye C/H -forhold, når aromatiske hydrokarboner blir brent ildgule flammer, er produktet av kullpartiklene dannet (sot).
Erstatningsreaksjoner
Aromatiske hydrokarboner kan erstatte hydrogenatomer med andre substituenter. Dette oppnås gjennom to typer organiske reaksjoner: aromatisk elektrofil substitusjon (Sear), eller aromatisk nukleofil substitusjon (SNAR).
Dufter
Aromatiske hydrokarboner, som navnet antyder, er preget av å ha søte eller sterke lukter. Denne egenskapen tillot dem å differensiere dem, i prinsippet, fra gassformige hydrokarboner og noen bille -parafiner.
Eksempler på aromatiske hydrokarboner
Aromatiske hydrokarboner, strengt tatt, bekymrer bare de som er sammensatt av karbon og hydrogen. Det skal ikke være noen heteroátomos (eller, p, n, s, etc.). Derfor forlater følgende eksempler som vil bli nevnt til forbindelser som pyridin, furano eller fenol.
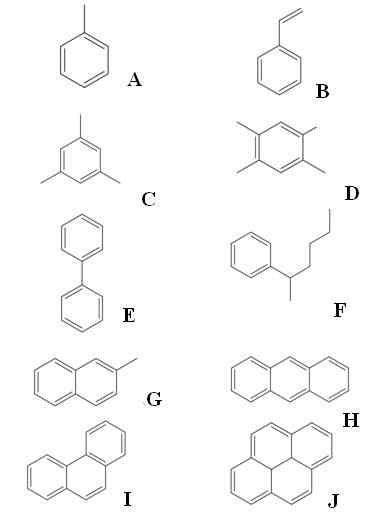 Eksempler på aromatiske hydrokarboner. Kilde: Gabriel Bolívar via Molview.
Eksempler på aromatiske hydrokarboner. Kilde: Gabriel Bolívar via Molview. Opp har vi ti eksempler på aromatiske hydrokarboner. Merk at alle har minst en benzenisk ring. Navnene deres er:
A: Toluen
B: Strekk
C: Mesitileno
D: Sent
E: Bifenyl
F: 2-fenilhexan
G: 2-metylnaftalen
H: Anthracen
I: Fenantreno
J: Pireno
Av dem alle er toluen den med størst industriell verdi.
Applikasjoner/bruksområder
De fleste anvendelser av aromatiske hydrokarboner består av å tjene som råstoff for syntese, eller produksjon, produkter med høy kommersiell verdi. Nesten alle av dem starter fra benzen, som blir utsatt for flere organiske reaksjoner for å oppnå funksjonelle derivater.
Fibre og plast
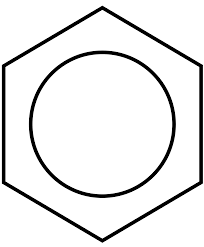 Benzen
Benzen Fra benzen er det cykloheksan, som deretter blir transformert til andre forbindelser for å syntetisere nylon 6 eller nylon 66. På den annen side kan strekningen også fås fra benzenet, som består av polystyrenmonomeren. Dermed har vi polymerer som er nødvendige for produksjon av fibre og plast.
Kan tjene deg: aktiveringsenergiEpoksyharpikser
Fra benzen kan også bisfenol A syntetiseres, som etter forskjellige syntese ruter, epoksyharpikser, lim, lim og til og med malerier forekommer.
Vaskemidler
Alkybentes med lange sidekjeder tjener til produksjon av vaskemidler; Blant dem, alkybenzeosulfonater.
TNT
Fra toluen kan du produsere TNT: Trinitrotoluen, en av de mest kjente eksplosivene.
Benzosyre
Fra toluen oppnås benzosyre som avledet, essensiell forbindelse for formuleringene av mange parfymer, medisiner og mat.
Løsningsmidler
Benzen, Toluen og Xileno (BTX), er de mest brukte organiske løsningsmidlene i oljeforskning.
Bensin
Aromatiske hydrokarboner er også en del av sammensetningen av bensin, med hovedrollen som å heve dens oktan- eller oktanindeks.
Referanser
- Graham Solomons t.W., Craig f. Yngel. (2011). Organisk kjemi. (10th Utgave.). Wiley Plus.
- Carey f. (2008). Organisk kjemi. (Sjette utgave). Mc Graw Hill.
- Morrison og Boyd. (1987). Organisk kjemi. (Femte utgave). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Aromatisk forbindelse. Hentet fra: i.Wikipedia.org
- Ed Vitz et al. (8. september 2020). Aromatiske hydrokarboner. Kjemi librettexts. Gjenopprettet fra: Chem.Librettexts.org
- Wyman Elizabeth. (2020). Aromatiske hydrokarboner: Definisjon, eksempel og bruk. Studere. Gjenopprettet fra: Studie.com
- Boluda, ca. J., Macías, m., & González Marrero, J. (2019). Den kjemiske kompleksiteten til bilbensin. Vitenskap, ingeniørfag og applikasjoner,2(2), 51-79. Doi: doi.org/10.22206/Cyap.2019.V2i2.PP51-79
- « Bevaring av det lineære momentia -prinsippet, eksempler, øvelser.
- Bønner med G -eksempler og bruksregler »

