Perrin atommodellkarakteristikker, postulerer
- 1897
- 528
- Jonathan Moe
Han Perrin Atomic Model sammenlignet strukturen til atomet med et solsystem, der planetene ville være de negative belastningene og solen ville være en positiv belastning konsentrert i midten av atomet. I 1895 demonstrerte den enestående franske fysikeren overføringen av negative belastninger med katodestråler mot overflaten de påvirker.
Med dette ble den elektriske karakteren av katodestays demonstrert og ga lys på atomets elektriske natur, og forsto det som den minste og mest udelelige saken. I 1901 antydet Jean Baptiste Perrin at tiltrekningen av de negative belastningene rundt sentrum (positiv ladning) blir motvirket av treghetskraften.
 Jean Baptiste Perrin
Jean Baptiste Perrin Denne modellen ble komplementert og deretter perfeksjonert av Ernest Rutherford, som sa at hele den positive belastningen på atomet var lokalisert i midten av atomet, og at elektronene bane var rundt.
Imidlertid hadde denne modellen noen begrensninger som ikke kunne forklares den gangen, og modellen ble tatt som grunnlag av den danske fysikeren Niels Bohr for å foreslå sin modell i 1913.
[TOC]
Perrin atommodellkarakteristikker
De mest fremragende egenskapene til atom -atommodellen er følgende:
- Atomet består av en stor positiv partikkel i midten av det, der det meste av atommassen er konsentrert.
- Rundt denne konsentrerte positive belastningen går i bane rundt flere negative belastninger som kompenserer for den totale elektriske ladningen.
 Illustrasjon av atommodellen Perrin
Illustrasjon av atommodellen Perrin Perrins forslag sammenligner med atomstrukturen med et solsystem, der den positive positive belastningen ville oppfylle solens funksjon og de omkringliggende elektronene ville oppfylle planetens rolle.
Kan tjene deg: Ester LinkPerrin var banebrytende for å antyde atomets diskontinuerlige struktur i 1895. Imidlertid insisterte han aldri på å utforme et eksperiment som bidro til å bekrefte denne unnfangelsen.
Eksperiment
Som en del av doktorgraden hans fungerte Perrin som fysikkassistent for Normal School of Paris, mellom 1894 og 1897.
Da utviklet Perrin mesteparten av sin undersøkelse av å verifisere katodestrålene; det vil si hvis katodestrålene var elektrisk ladede partikler, eller hvis de tok formen på bølgene.
Katodestråler
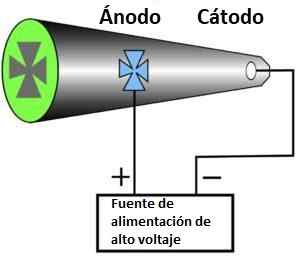
Eksperimentet med katodestråler oppstår når du gjennomfører undersøkelser med Crookes -rør, en struktur oppfunnet av den engelske kjemikeren William Crookes på 1870 -tallet.
Crookes -røret består av et glassrør som bare inneholder gasser inni. Denne konfigurasjonen har et metallstykke i hver ende, og hvert stykke er koblet til en ekstern spenningskilde.
Når røret er energisk, ioniseres luften inni.

Inne.
Da var det ukjent om fluorescensen skyldtes sirkulasjonen av elementære partikler i røret, eller om strålene adopterte formen på bølgene som transporterte dem.
Perrins undersøkelser
I 1895 svarte Perrin at katode Ray -eksperimenter som forbinder et nedlastingsrør til en tom større beholder.
I tillegg plasserte Perrin en vanntett vegg for vanlige molekyler og svarte Crookes -konfigurasjonen ved å plassere et Faraday -bur, inneholdt i et beskyttende kammer.
Kan tjene deg: natrium: historie, struktur, egenskaper, risikoer og brukHvis strålene krysset den vanntette veggen for vanlige molekyler inne i Faraday -buret, ville det automatisk demonstrert at katodestrålene var sammensatt av elektrisk ladede grunnleggende partikler.
Bekreftelsesmetode
For å bekrefte dette, koblet perrin et elektrometer nær den vanntette veggen for å måle de elektriske belastningene som ville oppstå når katodestrålene påvirker der.
Når man utførte eksperimentet, ble det bevist at sammenstøtet med katodestråler mot den vanntette veggen induserte en liten negativ belastningsmåling i elektrometeret.
Deretter avledet perrin strømmen av katodestråler som tvang systemet ved induksjon av et elektrisk felt, og tvang katodestrålene til å påvirke elektrometeret. Da det skjedde, registrerte måleren en betydelig overlegen elektrisk kostnad sammenlignet med forrige registrering.
Takket være Perrins eksperimenter ble det vist at katodestråler var sammensatt av partikler med negativ belastning.
Deretter, på begynnelsen av 1900 -tallet, J. J. Thomson oppdaget formelt eksistensen av elektroner og deres last-masa-forhold, basert på Perrins undersøkelser.
Postulater
I 1904 den britiske forskeren J.J. Thomson uttalte forslaget sitt som en atommodell, også kjent som Plum's Pudding -modellen.
I denne modellen ble den positive belastningen forstått som en homogen masse, og de negative ladningene ville bli tilfeldig spredt over nevnte positiv masse.
I analogien ville den positive belastningen være masse av kompisen, og de negative ladningene ville bli representert av plommene. Denne modellen ble tilbakevist av Perrin i 1907. I sitt forslag indikerer Perrin følgende:
- Den positive belastningen utvides ikke gjennom hele atomstrukturen. Tvert imot, det er konsentrert i midten av atomet.
- Negative ladninger er ikke spredt gjennom atomet. På den annen side er disse plassert på en ordnet måte rundt den positive belastningen, mot atomets ytterkant.
Begrensninger
Perrins atommodell har to hovedbegrensninger, som deretter ble overvunnet takket være bidragene fra Bohr (1913) og kvantefysikk.
De viktigste begrensningene i dette forslaget er:
- Det er ingen forklaring på hvorfor den positive belastningen forblir konsentrert i midten av atomet.
- Stabiliteten til banene for de negative belastningene rundt atomets sentrum er ikke forstått.
- I følge Maxwells elektromagnetiske lover, vil negative belastninger beskrive spiralbaner rundt positive ladninger, inntil de kolliderer med disse.
Artikler av interesse
Schrödinger atommodell.
Broglie Atomic Model.
Chadwick Atomic Model.
Heisenberg Atomic Model.
Thomson Atomic Model.
Dalton Atomic Model.
Dirac Jordan Atomic Model.
Democritus Atomic Model.
Leucipo atommodell.
Bohr atommodell.
Gjeldende atommodell.
Referanser
- Jean Perrin (1998). Encyclopædia Britannica, Inc. Gjenopprettet fra: Britannica.com
- Jean Baptiste Perrin (20014). Encyclopedia of World Biography. Gjenopprettet fra: Encyclopedia.com
- Kubbinga, h. (2013). En hyllest til Jean Perrin. © European Physical Society. Gjenopprettet fra: EurophysicsNews.org
- Atomic Model (S.F.). Havana Cuba. Gjenopprettet fra: ECURED.Cu
- Perrin, J (1926). Diskontinuerlig struktur av materie. Media Ab Nobel. Gjenopprettet fra: Nobelprize.org
- Solbes, J., Silvestre, v. Og furió, c. (2010). Den historiske utviklingen av atom- og kjemiske bindingsmodeller og deres didaktiske implikasjoner. University of Valencia. Valencia Spania. Hentet fra: OJS.UV.er

