Metylsalicylat
- 1623
- 366
- Prof. Oskar Aas
Hva er metylsalisylat?
Han Metylsalicylat Det er et kjemikalie, av organisk natur, betraktet som forbindelsen med større toksisitet blant de kjente salisylater, til tross for dens fargeløse og behagelige lukt med en svak søt berøring. Denne arten er bedre kjent under navnet Gaulteria Oil. Formelen er c8H8ENTEN3.
Det er i en flytende tilstand i standard temperatur- og trykkforhold (25 ° C og 1 atm), og utgjør en organisk ester som naturlig stammer fra et bredt utvalg av planter. Fra observasjon og studie av dens produksjon i naturen var det mulig å gå videre til syntesen av metylsalisylat.
Denne syntesen ble utført ved hjelp av en kjemisk reaksjon mellom esteren fra salisylsyren og dens kombinasjon med metanol. På denne måten er denne forbindelsen en del av vismannen, hvitvin og frukt som plomme og eple, blant andre funnet naturlig.
Syntetisk, metylsalisylat brukes til produksjon av aromatiserende midler, så vel som i visse måltider og drikke.
Kjemisk struktur
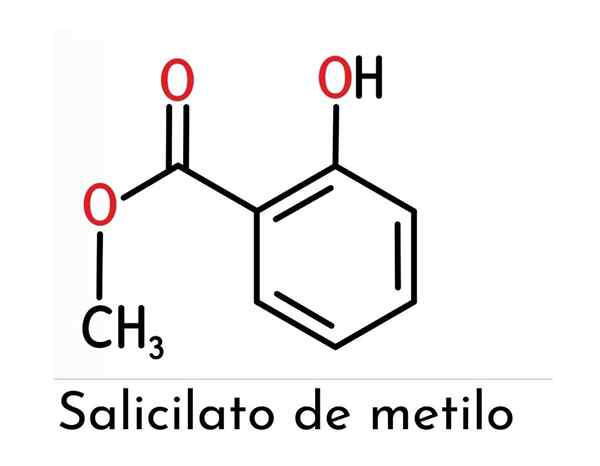
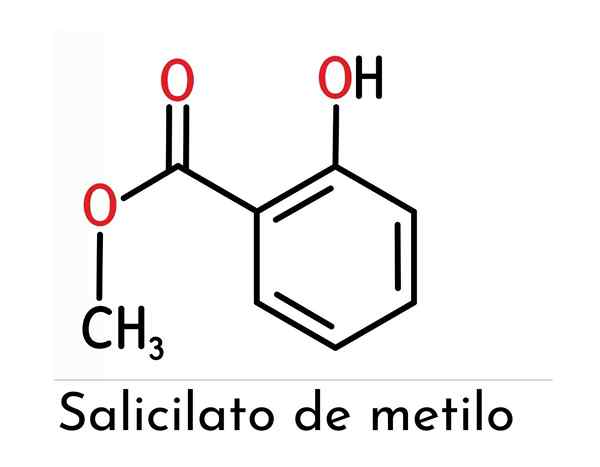
Den kjemiske strukturen til metylsalisylat utgjøres av to hovedfunksjonelle grupper (en ester og en fenol festet til dette), som vist i det overordnede bildet.
Det observeres at det utgjøres av en benternisk ring (som representerer en direkte innflytelse på reaktiviteten og stabiliteten til forbindelsen), fra salisylsyren som den er avledet.
For å nevne dem hver for seg, kan det sies at de er forent i en orto -stilling (1.2) en hydroksylgruppe og en metylester til den nevnte ringen.
Kan tjene deg: Tertiær alkohol: struktur, egenskaper, eksemplerSå ettersom OH -gruppen er knyttet til benzenringen, dannes en fenol, men gruppen som har det største "hierarkiet" i dette molekylet er esteren, og gir en spesiell struktur til denne forbindelsen og derfor ganske spesifikke egenskaper.
Dermed blir det kjemiske navnet presentert som 2-hydroksybenzoat av metyl, gitt av IUPAC, selv om det er mindre ofte brukt når man refererer til denne forbindelsen.
Egenskaper til Metylsalicylat
- Det er en kjemisk art som tilhører gruppen av salisylater, som er produkter av naturlig opprinnelse fra metabolismen til noen planteorganismer.
- Det er kunnskap om de terapeutiske egenskapene til salisylater i medisinske behandlinger.
- Denne forbindelsen er til stede i visse drinker som hvitvin, te, salvie og visse frukt som papaya eller kirsebær.
- Det finnes naturlig i bladene til et stort antall planter, spesielt i visse familier.
- Det tilhører gruppen av organiske estere som kan syntetiseres i laboratoriet.
- Det oppnås i flytende tilstand, hvis tetthet er omtrent 1 174 g/ml i standardtrykk og temperaturforhold (1 atm og 25 ° C).
- Det danner en fargeløs, gulaktig eller rødlig væskefase, betraktet som vannløselig (som er et uorganisk løsningsmiddel) og i andre organiske løsningsmidler.
- Kokepunktet er omtrent 222 ° C, og manifesterer den termiske nedbrytningen rundt 340 til 350 ° C.
- Den presenterer flere applikasjoner, alt fra aromatiserende middel i godteriindustrien til smertestillende og andre produkter i legemiddelindustrien.
Kan tjene deg: natrium azid (NAN3): struktur, egenskaper, bruksområder, risiko- Dens molekylære formel er representert som C8H8ENTEN3 Og den har en molmasse på 152,15 g/mol.
Bruk/applikasjoner
På grunn av dens strukturelle egenskaper, som er en metylester fra salisylsyre, har metylsalisylat et stort antall bruksområder i forskjellige områder.
En av hovedbrukene (og den mest kjente) av dette stoffet er det av aromatiserende middel i forskjellige produkter: fra den kosmetiske industrien som en duft til matindustrien som smakstilsetning i søtsaker (tyggegummi, godteri, is, blant andre).
Det brukes også i kosmetikkindustrien som et oppvarmingsmiddel og for muskelmassasjer i sportsapplikasjoner. I sistnevnte tilfelle fungerer det som en rarefaktorisk; det vil si at det forårsaker overflaten rødhet i huden og membranene i slimhinnen når de kommer i kontakt med disse.
På samme måte brukes den i krem til aktuell bruk, for dens smertestillende og anti -inflammatoriske egenskaper i behandlinger for revmatiske forhold.
En annen av applikasjonene inkluderer dens flytende bruk i aromaterapi -økter, på grunn av dens essensielle oljeegenskaper.
I tillegg til bruken som et middel for beskyttelse mot ultrafiolett stråling i solkremer, blir dens egenskaper foran lyset for teknologiske anvendelser undersøkt, for eksempel produksjon av laserstråler eller å skape sensitive arter for å lagre informasjon i molekylene.
Syntese av Metylsalicylat
For det første skal det nevnes at metylsalisylat kan oppnås naturlig fra destillasjonen av grenene til visse planter, slik som Gaulteria (Gaultheria procumbens) eller søt bjørk (Langsom betula).
Det kan tjene deg: Ingen metaller: Historie, egenskaper, grupper, bruksområderDette stoffet ble trukket ut og isolert for første gang i 1843 takket være forskeren av fransk opprinnelse kalt Auguste Cahours; Fra Gaulteria er det for tiden oppnådd gjennom laboratorier syntese og til og med kommersiell.
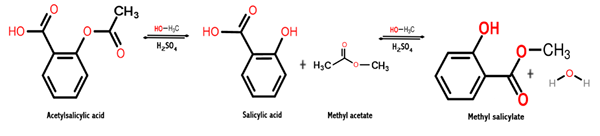
Reaksjonen som er gitt for å oppnå denne kjemiske forbindelsen er en prosess som kalles esterifisering, der en ester oppnås ved reaksjon mellom en alkohol og en karboksylsyre. I dette tilfellet oppstår det mellom metanol og salisylsyre, som vist nedenfor:
Ch3Oh + c7H6ENTEN3 → c8H8ENTEN3 + H2ENTEN
Det skal bemerkes at den delen av salisylsyremolekylet som er forestret med hydroksyl (OH) alkohol.
Så det som skjer mellom disse to kjemiske artene er en kondensasjonsreaksjon, fordi vannmolekylet fjernes blant reaktantene mens de andre reagerer arten blir kondensert for å oppnå metylsalisylat.
Følgende bilde viser syntese av metylsalisylat fra salisylsyre, der to påfølgende reaksjoner vises.