Valina -egenskaper, funksjoner, rik mat, fordeler
- 3954
- 279
- Jonathan Moe
De Valina Det tilhører de 22 aminosyrene som er identifisert som de "grunnleggende" komponentene i proteiner; Det er identifisert med forkortelsen "Val" og med brevet "V". Denne aminosyren kan ikke syntetiseres av menneskekroppen, derfor er den katalogisert i gruppen av ni essensielle aminosyrer for mennesker.
Mange kuleproteiner har et interiør rike på valine og leucinavfall, siden begge er assosiert med hydrofobe interaksjoner og er uunnværlige for folding av strukturen og den tre -dimensjonale konformasjonen av proteiner.
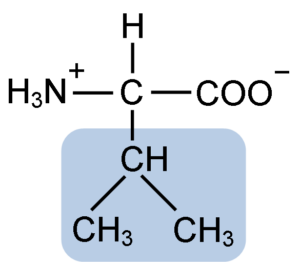 Kjemisk struktur av aminosyre Valine (kilde: Clavecin [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)] via Wikimedia Commons)
Kjemisk struktur av aminosyre Valine (kilde: Clavecin [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)] via Wikimedia Commons) La Valina ble renset for første gang i 1856 av V. Grup-Besanez fra et vandig ekstrakt av bukspyttkjertelen. Imidlertid ble navnet "Valina" myntet av E. Fisher i 1906, da han klarte å syntetisere den kunstig og observerte at strukturen var veldig lik den av verdsettelse, funnet i planter som ofte er kjent som "Valerianas".
Valinen er en av aminosyrene som finnes i posisjoner som er bevart i visse proteiner som deles av virveldyr, for eksempel i 80 plassering av cytokrom c av virveldyr er leucin, valin, isoleucin og metodin i samme rekkefølge i samme rekkefølge.
I vev eller biomaterialer med resistente, harde og elastiske egenskaper som leddbånd, sener, blodkar, tråder eller nett, er det store mengder valine, som gir fleksibilitet og motstand takket være dens hydrofobe interaksjoner med andre aminosyrer.
En erstatning av en glutamatrester med en av valin i β -kjeden av hemoglobin, proteinet som er ansvarlig for transport av oksygen ved blod forårsaker dårlig dannelse i proteinstrukturen, som forårsaker hemoglobin "S".
Denne mutasjonen produserer falciforme anemi eller drerepanocytose, en patologisk tilstand der røde blodlegemer skaffer seg en form for halvmåne eller karakteristisk HOZ, som skiller dem fra normalt, avrundet og flatet utseende.
Noen av de mest brukte ugressmidlene har for tiden aktive forbindelser til sulfonylurea og metylsulfometuron, som forårsaker skade på enzymet acetolaktatsyntase, nødvendig for det første trinnet med syntese av valin, leucin og isoleucin. Skadene forårsaket av disse plantevernmidlene forhindrer urter og ugress kan normalt utvikle seg.
[TOC]
Kjennetegn
Valina er en aminosyre med et fem -karbon skjelett og tilhører aminosyregruppen med alifatiske sidekjeder. Dens hydrofobe karakter er slik at den kan sammenlignes med fenylalanin, den av leucin og isoleucin.
Aminosyrer som har hydrokarbonkjeder i sine r eller sidekjeder, er ofte kjent i bibliografi som forgrenede eller forgrenede kjede aminosyrer. I denne gruppen er Valine, fenylalanin, leucin og isoleucin.
Generelt brukes aminosyrene i denne gruppen som indre strukturelle elementer i proteinsyntese, da disse kan assosieres med hverandre gjennom hydrofobe interaksjoner, "flyktende" fra vann og etablere den karakteristiske strukturelle foldingen av mange proteiner.
Molekylvekten er rundt 117 g/mol, og siden dens R- eller sidekjedegruppe er en forgrenet hydrokarbon, har den ingen belastning og dens relative overflod i proteinstrukturer er lite større enn 6%.
Struktur
La Valina deler den generelle strukturen og de tre typiske kjemiske gruppene av alle aminosyrer: karboksylgruppen (COOH), aminogruppen (NH2) og et hydrogenatom (-h). I sin R- eller sidekjedegruppe har den tre karbonatomer som gir den veldig hydrofobe egenskaper.
Kan tjene deg: inerte vesener: egenskaper, eksempler, forskjeller med levende vesenerSom det er tilfelle for alle kjemiske forbindelser klassifisert som "aminosyrer", har valinen et sentralt karbonatom som er chiral, og som er kjent som α karbon, som de fire kjemiske gruppene nevnt.
IUPAC-navnet på Valine er 2-3-amino-3-Butanóic.
Alle aminosyrer finnes i D- eller L -formen, og valinen er intet unntak. Imidlertid er L-verdi-formen mye rikelig enn D-Valleine-formen, og i tillegg er den spektroskopisk mer aktiv enn formen D.
L-verdi er formen som brukes til dannelse av celleproteiner og er derfor av de to den biologisk aktive formen. Det oppfyller funksjoner som ernæringsmessig, mikronæringsstoff for planter, metabolitt for mennesker, alger, gjær og bakterier, blant mange andre funksjoner.
Funksjoner
Til tross for at han er en av de ni essensielle aminosyrene, spiller ikke Valina en ekstra rolle i sin deltakelse i proteinsyntese og som en metabolitt i sin egen nedbrytningsvei.
Imidlertid er klumpete aminosyrer som valin og tyrosin ansvarlige for fleksibiliteten til fibroin, hovedproteinkomponenten i silketrådene produsert av arten av arten Bombyx Mori, ofte kjent som silke eller mulberry tre ormer.
Vev som arterielle blodbånd og glass er sammensatt av et fibrøst protein kjent som elastin. Dette består av polypeptidkjeder med gjentatte sekvenser av glycin, alanin og valinaminosyrer, den viktigste rest med protein.
Valina deltar i de viktigste synteseveiene til forbindelsene som er ansvarlige for den karakteristiske lukten av frukt. Valina -molekyler blir transformert til metylert og forgrenede derivater av estere og alkoholer.
I matindustrien
Det er mange kjemiske tilsetningsstoffer som bruker Valine i kombinasjon med glukose for å oppnå appetittvekkende lukt i visse kulinariske preparater.
Ved en temperatur på 100 ° C har disse tilsetningsstoffene en karakteristisk lukt av rug og mer enn 170 ° C -lukt i varm sjokolade, så de er populære innen matproduksjon i baker- og konditorindustrien (Pastry).
Disse kjemiske tilsetningsstoffene bruker kunstig syntetisert L-valin.
Biosyntese
Alle forgrenede aminosyrer som valin, leucin og isoleucin er hovedsakelig syntetisert i planter og bakterier. Noe som betyr at dyr som menneske og andre pattedyr trenger å innta mat som er rike på disse aminosyrene for å kunne oppfylle ernæringskravene sine.
Vanligvis begynner biosyntesen av valinen med overføring av to karbonatomer fra hydroksyetyltyaminpyrofosfat til pyruvatet ved virkningen av enzymet ocetohydroxi -isomersyre reduktasesyre.
De to karbonatomene stammer fra et andre pyruvatmolekyl gjennom en TPP-avhengig reaksjon som er veldig lik den som er katalysert av enzymet disarboxylase-pyruvat, men som katalyseres av dihydroxy-syrdehydratase.
Enzymet Valina aminotransferase inkluderer til slutt en aminogruppe i ketoacidforbindelsen som følge av den fremre dekarboksyleringen, som danner L-valin. Leucin-, isoleucin- og valinaminosyrer har en stor strukturell likhet, og dette er fordi mange mellommenn og enzymer deler på sine biosyntetiske ruter.
Det kan tjene deg: Flora og Fauna de Salta: Mer representative arterKetoacid produsert under biosyntesen av L-Valine regulerer noen enzymatiske trinn ved negativ tilbakemelding eller alosterisk regulering på den biosyntetiske ruten til leucin og andre relaterte aminosyrer.
Dette betyr at biosyntetiske ruter blir hemmet av en metabolitt generert i dem som, når de akkumuleres, gir celler et spesifikt signal som forteller dem at en viss aminosyre er i overkant og derfor kan syntesen stoppe.
Nedbrytning
De tre første nedbrytningstrinnene i valinen deles på nedbrytningsveien til alle forgrenede aminosyrer.
Valina kan komme inn i Krebs sitronsyresyklus for å bli transformert til succinyl-CoA. Nedbrytningsveien består av en innledende transaminering, katalysert av et enzym kjent som aminotransferase av forgrenede kjedeaminosyrer (BCAT).
Dette enzymet katalyserer en reversibel transaminering som klarer å konvertere den forgrenede kjede aminosyrene til deres tilsvarende forgrenede kjede α-Zo-Stoats.
I denne reaksjonen er deltakelsen av glutamat/2-zotoglutaratmoment essensielt, siden 2-Zotoglutarat mottar aminogruppen som fjernes fra aminosyren som blir metabolisert og blir glutamat.
Dette første reaksjonstrinnet i katabolismen til valinen produserer 2-metoisavalerat og er ledsaget av konvertering av pyridoksal 5'-fosfat (PLP) i pyridoksamin 5'-fosfat (PMP).
Deretter brukes 2-kolisvaleratet som et underlag av et mitokondrielt enzymatisk kompleks, kjent som α-a-Zo-stoats av forgrenet kjede, som tilfører en koksdel og danner Isobutiril-CoA, som deretter er dehydrogenert og snudd til metakrilil. -Coa.
Metakrylil-CoA blir behandlet nedstrøms i 5 ekstra enzymatiske trinn som involverer hydrering, eliminering av Coash-delen, oksidasjon, tilsetning av en annen koash-del og molekylær omorganisering, som ender med produksjonen av succinyl-CoA, som umiddelbart går inn i syklusen av Krebs.
Mat rik på Valina
Proteinene i sesam- eller sesamfrø er rike på Valina, med nesten 60 mg av aminosyren for hvert gram protein. Av denne grunn anbefales informasjonskapsler, kjeks og sesamstenger eller nougat for barn med mangelfulle dietter av denne aminosyren.
Soyakorn er generelt rike på alle essensielle aminosyrer, selv i Valina. De er imidlertid dårlige i metionin og cystein. Proteinet eller soyastrukturen har veldig komplekse kvartære strukturer, men som er enkle å oppløse og skille seg inn i mindre underenheter i nærvær av gastrisk juice.
Kasein, som vanligvis er i melk og dets derivater, er rik på gjentatte sekvenser av Valina. Som soyabønner blir dette proteinet lett degradert og absorbert i tarmkanalen til pattedyr.
Det er anslått at for hvert 100 gram soyaprotein blir det inntatt omtrent 4,9 gram valine; Mens for hver 100 ml melk, blir det inntatt omtrent 4,6 ml Valina.
Andre matvarer som er rike på nevnte aminosyre, er storfekjøtt, fisk og forskjellige typer grønnsaker og grønnsaker.
Fordelene med inntaket ditt
Valine er, som en stor del av aminosyrer, en glykogen aminosyre, det vil si at den kan integreres i den glukoneogene ruten, og mange nevrologer bekrefter at inntaket deres hjelper til med å opprettholde mental helse, muskulær koordinering og redusere stress.
Kan tjene deg: De 5 grenene til hovedbiotechnologienMange idrettsutøvere bruker komprimert komprimert i Valina, siden de hjelper regenerering av vev, spesielt muskelvev. Å være en aminosyre som er i stand til å bli sammen med glukoneogenese, hjelper energiproduksjon, noe som ikke bare er viktig for fysisk aktivitet, men for nervøs funksjon.
Valina -matvarer er med på å opprettholde balansen mellom nitrogenforbindelser i kroppen. Denne balansen er avgjørende for generering av energi fra proteinene som er inntatt, for kroppsvekst og helbredelse.
Forbruket forhindrer skade på leveren og galleblæren, samt bidrar til optimalisering av mange kroppsfunksjoner.
En av de mest populære kosttilskuddene mellom idrettsutøvere for å øke muskelvolum og muskelgjenoppretting er BCAA.
Disse typene tabletter består av tabletter med blandinger av forskjellige aminosyrer blant dem er generelt inkludert aminosyrer som L-valin, L-isoleucin og L-Leucina; De er også rike på vitamin B12 og andre vitaminer.
Noen eksperimenter med griser har vist at kravene til valin.
Mangelforstyrrelser
Daglig valineinntak anbefalt for spedbarn er rundt 35 mg for hvert gram proteinforbruk, mens for voksne er mengden litt lavere (rundt 13 mg).
Den vanligste sykdommen relatert til valin og andre forgrenede aminosyrer er kjent som "urinsykdom med arce sirup" eller "ketoaciduria".
Dette er en arvelig tilstand forårsaket av en defekt i genene som koder.
I denne sykdommen kan ikke organismen assimilere noen av disse tre aminosyrene når de oppnås fra kostholdet, derfor akkumuleres avledede ketoacider og blir utvist i urinen (de kan også påvises i blodserumet og i cerebrospinalvæsken).
På den annen side har et dårlig kosthold i Valina vært relatert til nevrologiske patologier som epilepsi. Det kan også forårsake vekttap, Huntingtons sykdom og kan til og med havne i utviklingen av visse typer kreft, siden vevsreparasjonssystemet og syntesen av biomolekyler blir kompromittert.
Referanser
- Abu-Baker, s. (2015). Gjennomgang av biokjemi: konsepter og forbindelser
- Nelson, d. L., Lehninger, a. L., & Cox, m. M. (2008). Lehninger prinsipper for biokjemi. Macmillan.
- Plimmer, r. H. TIL., & Phillips, h. (1924). Analysen av proteiner. Iii. Estimering av histidin og tyrosin ved bominering. Biochemical Journal, 18 (2), 312
- Plimmer, r. H. TIL. (1912). Den kjemiske konstitusjonen av proteiner (volum. 1). Longmans, grønt.
- Torii, k. TIL. Z. ELLER. ENTEN., & Iitaka, og. (1970). Krystallstrukturen til L-Valine. Crystallographica Seksjon B: Strukturell krystallografi og krystallkjemi, 26 (9), 1317-1326.
- Tosti, v., Bertozzi, f., & Fontana, l. (2017). Helsemessige fordeler med middelhavsdietten: metabolske og molekylære mekanismer. The Journals of Gerontology: Series A, 73 (3), 318-326.
- « Gravitasjonsenergiformler, egenskaper, applikasjoner, øvelser
- De 115 beste setningene om eleganse »

