Gulloksyd (iii) (AU2O3) Hva er struktur, egenskaper, bruk
- 2388
- 695
- Dr. Andreas Hopland
Han Gulloksid (III) Det er en uorganisk forbindelse med kjemisk formel er AU2ENTEN3. Teoretisk sett kunne naturen forventes utenfor den kovalente typen. Tilstedeværelsen av en viss ionisk karakter i dets faste stoffer kan imidlertid ikke utelukkes fullt ut; eller hva som er det samme, antar fraværet av au kation3+ ved siden av anion eller2-.
Det kan virke motstridende at gull, som er et edelt metall, kan oksidere. Under normale forhold kan ikke gullstykker oksidere ved kontakt med atmosfærenes oksygen; Men når de blir bestrålet med ultrafiolett stråling i nærvær av ozon, eller3, Panoramaet er en annen.
Hvis gullstjernene gjennomgår disse forholdene, ville de bli en rødbrun farge, karakteristisk for AU2ENTEN3.
Andre metoder for å oppnå dette oksidet ville innebære den kjemiske behandlingen av disse stjernene; For eksempel å gjøre deigen til gull til sitt respektive klorid, AUCL3.
Deretter til AUCL3, Og resten av de mulige dannet gullsalter, tilsettes et sterkt basismedium; Og med dette oppnås hydrert eller hydroksydoksyd, Au (OH)3. Endelig er den sistnevnte forbindelsen termisk dehydrert for å oppnå AU2ENTEN3.
Gulloksydstruktur (III)
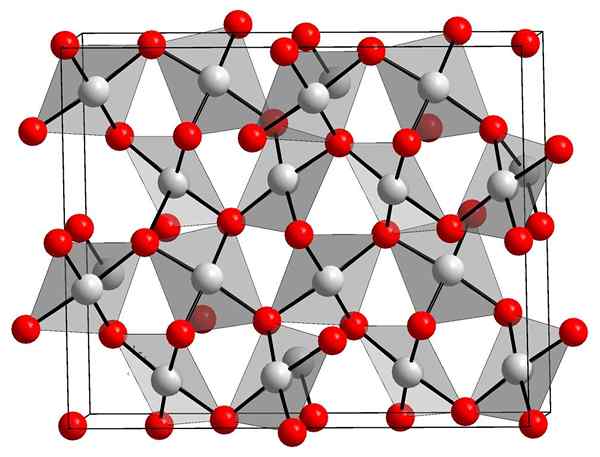
 Gulloksydkrystallinsk struktur. Orci, Wikimedia Commons.
Gulloksydkrystallinsk struktur. Orci, Wikimedia Commons. Det øvre bildet viser den krystallinske strukturen til gulloksyd (III). Disponering av gull- og oksygenatomer i det faste stoffet vises, enten med tanke på nøytrale atomer (kovalent faststoff), eller ioner (ionisk faststoff). Om hverandre, bare eliminere eller plassere AU-O-koblingene i alle fall.
I følge bildet antas det at den kovalente karakteren dominerer (som vil være logisk). Av den grunn er atomene og koblingene representert med henholdsvis sfærer og stenger. Hvite kuler tilsvarer gullatomer (AUIii-O), og de rødlige til oksygenatomer.
Kan tjene deg: hydroksyapatittHvis det blir observert nøye, vil det sees at det er AUO -enheter4, som binder med oksygenatomer. En annen måte å visualisere det på ville være å vurdere at hver AU3+ er omgitt av fire eller2-; Fra et ionisk perspektiv.
Denne strukturen er krystallinsk fordi atomer er bestilt ved å adlyde det samme lange rangeringsmønsteret. Dermed tilsvarer dens enhetlige celle det rhombohedrale krystallinske systemet (det samme som det øvre bildet). Derfor alle AU2ENTEN3 Det kan bygges hvis alle disse sfærene i enhetscellen ble fordelt i verdensrommet.
Elektroniske aspekter
Gull er et overgangsmetall, og det forventes at den. Denne overlappingen av orbitaler må teoretisk generere kjørebånd, noe som vil gjøre AU2ENTEN3 I et halvleder faststoff.
Derfor den sanne strukturen til AU2ENTEN3 er enda mer sammensatt med dette i tankene.
Hydrater
Golden Oxide kan beholde vannmolekyler inne i sine rhomboédicanical Crystals, noe som gir opphav til hydrater. Når slike hydrater dannes, blir strukturen amorf, det vil si uordentlig.
Den kjemiske formelen for slike hydrater kan være noe av følgende, som faktisk ikke er dypt avklart: AU2ENTEN3∙ Zh2O (z = 1, 2, 3 osv.), AU (OH)3, eller auxENTENog(ÅH)z.
AU (OH) -formelen3 representerer en forenkling av den sanne sammensetningen av disse hydratene. Dette er fordi innen gullhydroksid (III) også har funnet tilstedeværelsen av AU2ENTEN3; Og derfor mister det betydningen å behandle den isolert som en "enkel" overgangsmetallhydroksid.
Kan tjene deg: væskedampbalansePå den annen side, av et fast stoff med AU -formelxENTENog(ÅH)z En amorf struktur kunne forventes; Siden dette avhenger av koeffisientene x, og og z, hvis variasjoner ville resultere i alle typer struktur som knapt kan utvise et krystallinsk mønster.
Egenskaper
Fysisk utseende
Det er et rødbrunt faststoff.
Molekylmasse
441,93 g/mol.
Tetthet
11,34 g/ml.
Smeltepunkt
Den smelter og dekomponerer ved 160 ºC. Det mangler et kokepunkt, så dette oksidet koker aldri.
Stabilitet
Au2ENTEN3 Det er termodynamisk ustabilt fordi, som nevnt i begynnelsen, ikke har en tendens til å oksidere under normale temperaturforhold. Slik at det lett reduseres til å bli det edle gullet.
Jo høyere temperatur, jo raskere vil denne reaksjonen være, som er kjent som termisk nedbrytning. Dermed AU2ENTEN3 Ved 160 ºC bryter det ned for å produsere metallisk gull og frigjøre molekylært oksygen:
2 AU2ENTEN3 => 4 Au + 3 o2
En veldig lik reaksjon kan oppstå med andre forbindelser som favoriserer denne reduksjonen. Hvorfor reduksjon? Fordi gull får elektronene som oksygen fjernet; Hva er det samme som å miste koblinger til oksygen.
Løselighet
Det er et uoppløselig fast stoff i vann. Imidlertid er det løselig i saltsyre og salpetersyre, på grunn av dannelse av gullklorider og nitrater.
Nomenklatur
Gulloksydet (III) er navnet som styres av bestandens nomenklatur. Andre måter å nevne det på er:
-Tradisjonell nomenklatur: Auric Oxide, fordi Valencia 3+ er det største for gull.
-Systematisk nomenklatur: Dioro trioxide.
applikasjoner
Glassfarging
En av dens mest fremtredende bruk.
Kan tjene deg: hydrogenbromid (HBR)Syntese av aurater og fulminant gull
Hvis AU blir lagt til2ENTEN3 Til et medium der det er løselig, og i nærvær av metaller, kan det utfelle etter tilsetning av en sterk base auratene; som er dannet av AUO -anioner4- I selskap med metallkationer.
Også AU2ENTEN3 reagerer med ammoniakk for å danne den fulminante gullforbindelsen, AU2ENTEN3(NH3)4. Navnet hans stammer fra det faktum at det er svært eksplosivt.
Selvmontert monocapas manipulasjon
På gull og dets oksid adsorberes ikke visse forbindelser på samme måte, for eksempel disulfur dialil, RSSR. Når denne adsorpsjonen skjer, dannes en AU-S-binding spontant, der svovelatomet viser og definerer de kjemiske egenskapene til nevnte overflate avhengig av den funksjonelle gruppen den er koblet.
RSSR kan ikke adsorberes over AU2ENTEN3, Men om metallisk gull. Derfor, hvis overflaten av gull og dens oksidasjonsgrad blir modifisert, så vel som størrelsen på partiklene eller lagene til AU2ENTEN3, En mer heterogen overflate kan utformes.
Denne overflaten Au2ENTEN3-AUSR samhandler med metalloksider av visse elektroniske enheter, og utvikler dermed fremtidige smartere overflater.
Referanser
- Gulloksider. Gjenopprettet fra: 911 Metallurgist.com
- Shi, r. Asahi og c. Stampfl. (2007). Egenskapene til gulloksydene AU2ENTEN3 og au2O: Første prinsipper forskning. Det amerikanske fysiske samfunnet.
- « Chigualcan hva er, egenskaper, habitat, bruksområder, egenskaper
- Hemidesmosomes hva som er, beskrivelse, struktur, funksjoner »

