Natriumjodid (NAI) struktur, egenskaper, bruksområder, risiko

- 4321
- 545
- Anders Mathisen
Han natriumjodid Det er en uorganisk forbindelse dannet av et natrium Na -atom og et jodatom. Den kjemiske formelen er NAI. Det er et hvitt fast stoff som har en tendens til å absorbere vann fra miljøet, det vil si at det er hygroskopisk. Så hygroskopisk at det sies at det er delikoserende, for når tiden går, blir det oppløst i vannet som har absorbert.
Natriumjodid har flere bruksområder i medisinområdet, for eksempel tjener det til å gjøre bronkial sekresjoner mindre tykt (slim), så det brukes til å behandle bronkitt og astma.
 Fast nai natriumjodid. Ingen maskinlesbar forfatter gitt. Walkerma antatt (basert på copyright -krav). [Offentlig domene]. Kilde: Wikimedia Commons.
Fast nai natriumjodid. Ingen maskinlesbar forfatter gitt. Walkerma antatt (basert på copyright -krav). [Offentlig domene]. Kilde: Wikimedia Commons. Fordi elementet jod er et mikronæringsstoff for kroppen, brukes NAI natriumjodid i løsningene som blir injisert i pasienter som ikke kan mates gjennom munnen. Det brukes også i visse enheter som tjener til å oppdage sykdommer gjennom gammastråling.
Det har en viktig bruk i veterinærmedisin for å behandle forskjellige sykdommer hos dyr, hovedsakelig pattedyr. NAI brukes også som et reagens i organiske kjemilaboratorier.
[TOC]
Struktur
Natriumjodid dannes ved et natriumna -kation+ og en jodidanion i-, Derfor er det en ionisk forbindelse.
 Yoduro Anion i- (stor) og natriumkation na+ (litt). Claudio Pistilli [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikimedia Commons.
Yoduro Anion i- (stor) og natriumkation na+ (litt). Claudio Pistilli [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikimedia Commons. Jodidionet er mye større enn natriumionet, men i det faste stoffet er de perfekt koblet og danner kubikkkrystaller.
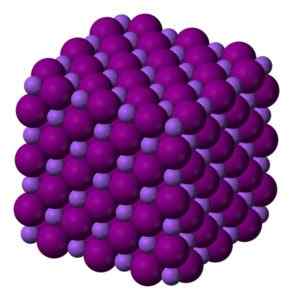 I det faste nai -glasset er natrium- og jodidioner perfekt koblet og danner et kubikkglass. Benjah-BMM27 [Public Domain]. Kilde: Wikimedia Commons.
I det faste nai -glasset er natrium- og jodidioner perfekt koblet og danner et kubikkglass. Benjah-BMM27 [Public Domain]. Kilde: Wikimedia Commons. Nomenklatur
Natriumjodid
Egenskaper
Fysisk tilstand
Hvitt fast stoff av delikatkrystaller (absorberer vann raskt fra miljøet). Kubikkkrystaller.
Molekylær vekt
149,89 g/mol
Kan tjene deg: Justus von LiebigSmeltepunkt
661 ° C
Kokepunkt
1304 ° C
Tetthet
3,67 g/cm3
Løselighet
Veldig løselig i vann: 184 g/100 ml vann ved 25 ° C. Alkoholoppløselig: 42,57 g/100 ml alkohol. Acetonoppløselig: 39,9 g/100 ml aceton.
Ph
8-9.5 (det tilberedes litt alkalisk for å være mer stabil).
Kjemiske egenskaper
Den blir brun hvis den blir utsatt for luften, da den frigjør jod i2. De vandige oppløsningene dine er på samme måte påvirket.
Natriumjodid nai reagerer med oksidasjonsmidler som produserer jod i2. Med veldig sterke oksidasjonsmidler som perklorsyre, kan reaksjonen være voldelig.
Andre egenskaper
Det er delikoserende, det vil si veldig hygroskopisk. Absorberer miljøfuktighet raskt. Kan absorbere opptil 5% av vannvekten.
Saltvannsmak og litt bitter.
Å skaffe
Natriumjodid kan oppnås fra jod I2 NaOH natriumhydroksyd. Det kan også fremstilles ved reaksjon mellom natriumkarbonat og en sur jodidløsning.
Bruker innen medisin
For astma og bronkittbehandling
NAI brukes som en slimløsende når det er veldig iherdige bronkialsekretser, den tjener til flytende.
 Bronkiene er den forgrenede delen av lungene. I noen tilfeller kan bronkitt behandles med natriumjodid. Forfatter: OpenClipart-vektorer. Kilde: Pixabay.
Bronkiene er den forgrenede delen av lungene. I noen tilfeller kan bronkitt behandles med natriumjodid. Forfatter: OpenClipart-vektorer. Kilde: Pixabay. Det brukes i bronkitt og astma. Det skal ikke administreres etter at hosten har "løsne". Men hos pasienter med kronisk bronkitt eller astma kan det foreskrives mer eller mindre kontinuerlig hvis lettelse oppnås.
I intravenøs mat
Natriumjodid er en kilde til jod og kan leveres som et supplement for total parenteral ernæring, som er en type intravenøs mat.
I diagnosen og behandlingen av skjoldbruskkjertelen
I sin radioaktive form har NAI blitt brukt som et diagnostisk verktøy for å evaluere skjoldbruskfunksjonen og strukturen til noen pasienter.
Kan tjene deg: periodisk bord, hva er det forNatriumjodidbehandling har blitt brukt til å behandle hypertyreose, men kontrollerer vanligvis ikke fullstendig manifestasjonene av sykdommen, og etter en stund forsvinner dens gunstige effekt.
Ved å fortsette behandlingen med jodid, kan hypertyreose kan vende tilbake til sin opprinnelige intensitet eller kan bli mer alvorlig enn i begynnelsen.
I gammakameraer
Gamma -kameraer er instrumenter som tillater å ta bilder avledet fra gammastråling. De brukes i nukleærmedisin for diagnose av noen sykdommer.
Gammakammeret bruker en natriumjodidkrystall som gamma strålingsdetektor fra pasienten, som har blitt injisert intravenøst en veldig liten mengde av et radioaktivt stoff.
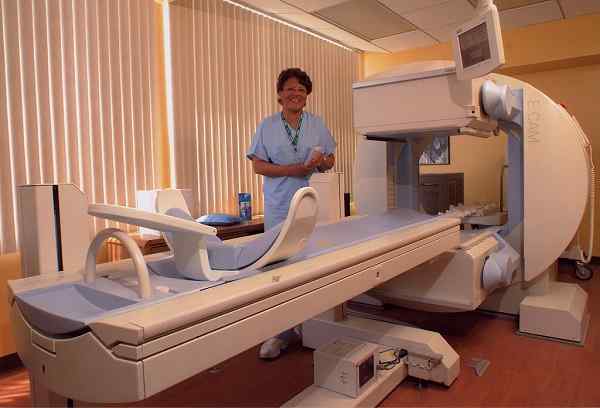 Gamma -kamerautstyr, som lar deg oppdage visse sykdommer gjennom gammastråling. Brendaicm [CC By-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]. Kilde: Wikimedia Commons.
Gamma -kamerautstyr, som lar deg oppdage visse sykdommer gjennom gammastråling. Brendaicm [CC By-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]. Kilde: Wikimedia Commons. I veterinærmedisin
I veterinærmedisin har det blitt brukt til å eliminere ringede ormer, i kreftlesjoner og ved visse inflammatoriske sykdommer hos hundene til hunder.
Det brukes til å behandle mykose, kroniske leddbetennelser, laryngitt, bronkitt og pleuritt hos noen arter av dyr. Det brukes til å fjerne ormer fra katter fra katter.
 Noen kattesykdommer kan behandles med natriumjodid. Forfatter: Skeze. Kilde: Pixabay.
Noen kattesykdommer kan behandles med natriumjodid. Forfatter: Skeze. Kilde: Pixabay. Det brukes også som et middel til x -løp av blære av noen dyr.
Natriumjodid brukes som hjelp i behandlingen av aktinomykose og aktinobacillose hos storfe (det kan være hos kyr, sauer og geiter).
Actinomycosis eller "gummi kjeve" er en infeksjon i kjevebenene, der beinene øker i størrelse, forårsaker smerter og dyret ikke kan mates riktig.
Actinobacillosis eller "tretunge" er en tungeinfeksjon som svulmer, og dyret kan ikke tygge mat.
Kan tjene deg: Svovelsyre (H2SO4)Natriumjodid bidrar med andre medisiner for å kurere begge sykdommer.
Natriumjodid brukes også som en slimløselig sykdom i kyr, hester og sauer.
 Noen sykdommer som påvirker kyr kan behandles med natriumjodid NAI. Forfatter: Ulrike Leone. Kilde: Pixabay.
Noen sykdommer som påvirker kyr kan behandles med natriumjodid NAI. Forfatter: Ulrike Leone. Kilde: Pixabay. Andre bruksområder
I organiske kjemiske reaksjoner
Natriumjodid var en av de første saltene som ble brukt til å gjøre det.
Å trekke ut forurenset sandmikroplastikk
Natriumjodid har blitt brukt til å trekke ut mikroplastikk (veldig små plastbiter) sand forurenset med dette materialet.
Mikroplastisk forurensning er observert i forskjellige naturlige miljøer, som elver, innsjøer, hav, hav, kyster og til og med i ubåtmiljøer, så det er en global bekymring.
Mikroplast blir inntatt av marine og landdyr som forårsaker alvorlig helseskade.
 Plast som blir kastet på strendene fører til høy forurensning av sand og hav. Med natriumjodid kan du måle hvor mye mikroplast det er i sanden. Forfatter: h. Hach. Kilde: Pixabay.
Plast som blir kastet på strendene fører til høy forurensning av sand og hav. Med natriumjodid kan du måle hvor mye mikroplast det er i sanden. Forfatter: h. Hach. Kilde: Pixabay. Målet på mengden mikroplast som et bestemt område har utføres ved å ta en del av sand og fordype den i natriumjodidløsningen.
På denne måten vil mikroplasten flyte. Natriumjodidløsninger har tilstrekkelig tetthet for plastmikropartikler for å flyte, til og med den tetteste plast.
Selv om natriumjodid er dyrt, blir metoder utviklet for å gjenbruke og redusere kostnadene ved denne prosedyren.
Risiko
Hvis natriumjodid kommer i kontakt med Hclo4 percloric acid.
Det er irriterende for øyne, hud- og luftveisanalen. Inntatt kan påvirke skjoldbruskkjertelen. Det kan forårsake sensibilisering i kroppen.
Det er skadelig for føttene til gravide, for hvis de inntar det eller inhalerer, kan det forårsake død for babyen eller veldig alvorlig og permanent skade.
Overdose i natriumjodid kan forårsake "jodisme" som er preget av overflødig spytt, nysing, konjunktivitt, hodepine, feber, laryngitt, blant andre symptomer.
Referanser
- ELLER.S. National Library of Medicine. (2019). Natriumjodid. Nasjonalt senter for bioteknologiinformasjon. Gjenopprettet fra Pubchem.NCBI.NLM.NIH.Gov.
- Cherry, s.R. et al. (2012). Gamma -kameraet. In Physics in Nuclear Medicine (fjerde utgave). Gjenopprettet fra Scientedirect.com.
- Kedzierski, m. et al. (2016). Effektiv mikroplastekstraksjon fra sand. En kostnadseffektiv metodikk basert på natriumjodidgjenvinning. Marine Pollution Bulletin 2016, utvunnet fra Elsevier.com.
- Van Meter, D.C. et al. (2008). Smittsomme sykdommer i mage -tarmkanalen. I Rebeuns ønsker av melkefe. Gjenopprettet fra Scientedirect.com.
- Stek, a.J. (1991). Reduksjon. I å forstå organisk syntese. Gjenopprettet fra Scientedirect.com.
- Young, J.TIL. (2004). Natriumjodid. Journal of Chemical Education, Vol. 81, nei. 3, mars 2004. Gjenopprettet fra puber.ACS.org.
- « Natriumsilikat (Na2SIO3) struktur, egenskaper, bruksområder, risikoer
- Omkretsen av sirkelen hvordan få den ut og formler, løste øvelser »

