Carnot Cycle Stages, applikasjoner, eksempler, øvelser
- 4171
- 932
- Prof. Oskar Aas
Han Carnot Cycle Det er sekvensen av termodynamiske prosesser som foregår i en Carnot -motor, en ideell enhet som bare består av reversible prosesser; det vil si at de som, etter å ha funnet sted, kan vende tilbake til den opprinnelige tilstanden.
Denne typen motor anses som ideell, siden den mangler spredning, friksjon eller viskositet som oppstår i virkelige maskiner, og gjør den termiske energien til brukbart arbeid, selv om konverteringen ikke er utført 100%.
 Figur 1. Et damplokomotiv. Kilde: Pixabay
Figur 1. Et damplokomotiv. Kilde: Pixabay En motor er bygget basert på et stoff som er i stand til å utføre arbeid, for eksempel gass, bensin eller damp. Dette stoffet er underlagt forskjellige temperaturendringer og opplever igjen variasjoner i trykket og volumet. På denne måten er det mulig å bevege et stempel inne i en sylinder.
[TOC]
Hva er Carnot -syklusen?
Carnot -syklusen foregår i et system som heter Carnot eller C -motor, som er en ideell gass låst i en sylinder og utstyrt med et stempel, som er i kontakt med to kilder ved forskjellige temperaturer t1 og T2 som den som er vist i følgende figur til venstre.
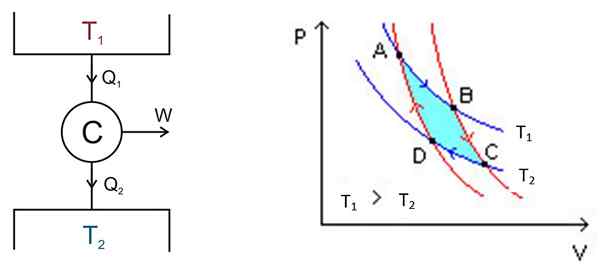 Figur 2. Til venstre et opplegg for C ARNOT -maskinen, til høyre PV -diagrammet. Kilde til venstre figur: Keta - eget arbeid, CC av 2.5, https: // Commons.Wikimedia.org/w/indeks.PHP?Curid = 681753, høyre figur Wikimedia Commons.
Figur 2. Til venstre et opplegg for C ARNOT -maskinen, til høyre PV -diagrammet. Kilde til venstre figur: Keta - eget arbeid, CC av 2.5, https: // Commons.Wikimedia.org/w/indeks.PHP?Curid = 681753, høyre figur Wikimedia Commons. Det er følgende prosesser i en grov modus:
- En viss mengde varme leveres til enheteninngang = Q1 Fra den termiske tanken ved høy temperatur t1.
- Carnot C -motoren utfører et verk med denne varmen som leveres.
- En del av varmen som ble brukt: avfallet qexit, Den overføres til den termiske tanken som er ved lavere temperatur t2.
Carnot Cycle Stages
Analysen er laget av et P -V -diagram (trykk -volum), som vist i figur 2 (høyre figur). Motorens mål kan være å holde termisk avsetning 2 kaldt, og trekke ut varmen fra den. I dette tilfellet er det en Kjølemedium. Hvis du tvert imot vil du gi varme til det termiske avsetningen 1, er det en Varmepumpe.
P -V -diagrammet viser trykkendringer - Motoremperatur under to forhold:
- Opprettholde den konstante temperaturen (isotermisk prosess).
- Ingen varmeoverføring (termisk isolasjon).
De to isotermiske prosessene må kobles til, som oppnås ved hjelp av termisk isolasjon.
Punkt
Du kan starte når som helst i syklusen, der gass har visse trykk, volum og temperaturforhold. Gassen lider av en serie prosesser og kan gå tilbake til startforholdene for å starte en annen syklus, og alltid er den endelige indre energien den samme som den første. Siden energi er bevart:
Arbeid utført av C = inngangsvarme - Avgangsvarme
Δw = qinngang - Qexit
Området som er inkludert i denne syklusen eller sløyfen, i turkis i figuren, tilsvarer nettopp arbeidet som er utført av Carnot -motoren.
Punkter A, B, C og D er merket i figur 2. Det vil begynne med poenget med å følge den blå pilen.
Første trinn: Isotermisk ekspansjon
Temperaturen mellom punktene A og B er T1. Systemet absorberer varme fra termisk avsetning 1 og lider av en isotermisk ekspansjon. Da øker volumet og trykket avtar.
Temperaturen forblir imidlertid i t1, siden når gassen utvides den avkjøles. Derfor forblir den indre energien konstant.
Det kan tjene deg: Graff Van Generator: Fester, hvordan det fungerer, applikasjonerAndre trinn: Adiabatisk utvidelse
På punkt B begynner systemet en ny utvidelse der systemet ikke vinner eller mister varmen. Dette oppnås ved å sette det i kaloriisolasjon som angitt før. Derfor er det en adiabatisk ekspansjon som fortsetter å peke C etter den røde pilen. Volumet øker og trykket avtar til det når sin laveste verdi.
Tredje trinn: Isotermisk komprimering
Start på punkt C og ende i D. Isolasjonen fjernes og systemet kommer i kontakt med termisk avsetning 2, hvis temperatur t2 Det er mindre. Systemet gir avfallsvarme til den termiske tanken, trykket begynner å øke og volumet for å avta.
Fjerde trinn: Adiabatisk komprimering
Nådd til punkt D, går systemet tilbake til termisk isolasjon, trykket øker og volumet avtar til det når de opprinnelige forholdene til punktet a. Da gjentas syklusen igjen.
Carnots teorem
Carnots teorem ble først postulert på begynnelsen av 1800 -tallet av den franske fysikeren Sadi Carnot. I året 1824 publiserte Carnot, som var en del av den franske hæren, en bok der han foreslo svaret på følgende spørsmål: Under hvilke forhold en termisk maskin har maksimal effektivitet? Carnot etablerte deretter følgende:
Ingen termisk motor som kjører mellom to termiske avsetninger er mer effektiv enn Carnot -motoren.
Η utbyttet av en termisk motor er gitt av forholdet mellom arbeidet som er utført w og den absorberte varmen Q:
ytelse = arbeid utført/varme absorbert
På denne måten er ytelsen til enhver termisk motor jeg: η = w/q. Mens ytelsen til en Carnot R -motor er η '= w/q', i tilfelle av begge motorene er de i stand til å utføre den samme jobben.
Carnots teorem uttaler at η aldri er større enn η '. Ellers faller det i strid med den andre loven om termodynamikk, hvor en prosess der resultatet er at varme fra et legeme med lavere temperatur er umulig å gå til en annen av høyere temperatur uten å motta ekstern hjelp. Derfor:
η < η'
Carnots teorem -demonstrasjon
For å vise at dette er slik, bør du vurdere Carnot -motoren som en kjøleskapsmaskin drevet av en I -motor. Dette er mulig siden Carnot -motoren fungerer etter reversible prosesser, som spesifisert i begynnelsen.
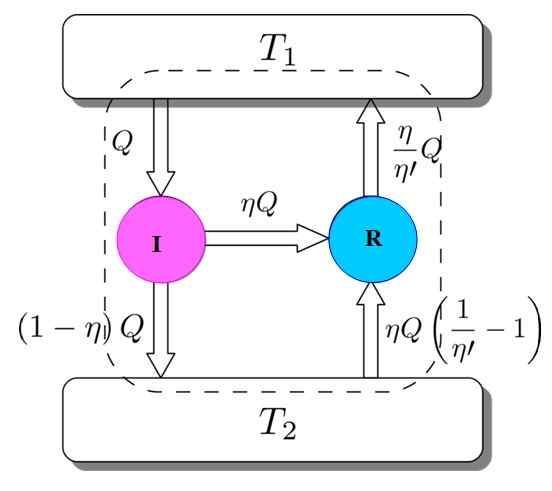
 Figur 3. Carnots teorem -demonstrasjon. Kilde: Netheril96 [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]
Figur 3. Carnots teorem -demonstrasjon. Kilde: Netheril96 [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)] Du har begge: Jeg og R jobber med de samme termiske forekomstene, og det vil antas at η > η'. Hvis en selvmotsigelse oppnås med den andre loven om termodynamikk, blir Carnots teorem demonstrert ved reduksjon til absurditet.
Figur 3 hjelper til med å følge prosessen. I -motoren tar en mengde varme Q, som deler seg på denne måten: å gjøre arbeid med r tilsvarer w = ηq og resten er varmen overført (1 -η) q til den termiske tanken t2.
Siden energien er bevart, er alt oppfylt:
OGinngang = Q = arbeid w + varme tildelt t2 = ηq + (1 -η) q = eexit
Nå tar Carnot R -kjøleskapsmaskinen den termiske tanken 2 en mengde varme gitt av:
Det kan tjene deg: imantasjon: hva som består, metode og eksempler(η / η ') (1 -η') q =
Energi må også oppbevares i dette tilfellet:
OGinngang = ηq + (η / η ') (1 -η') q = (η / η ') q = q' = eexit
Resultatet er overføringen til den termiske tanken T2 av en mengde varme gitt av (η / η ') q = q'.
Hvis η er større enn η 'betyr det at den høyeste temperaturens termiske avsetning har kommet mer varme enn jeg tok opprinnelig. Siden ingen ekstern middel, for eksempel en annen termisk kilde, har deltatt, er den eneste måten det kan skje at den kaldeste termiske avsetningen gir varmen.
Dette er uenig i den andre loven om termodynamikk. Det konkluderes da at det ikke er mulig at η' Være mindre enn η, derfor kan I -motoren ikke ha mer ytelse enn Carnot R -maskinen.
Teorem korollar og begrensninger
Carnot Theorem Corollary uttaler at to Carnot -maskiner har samme effektivitet hvis begge opererer med de samme termiske avsetningene.
Det betyr at stoffet ikke betyr noe, ytelsen er uavhengig og ikke kan heves ved å endre det.
Konklusjonen av den forrige analysen er at Carnot -syklusen er toppen av den ideelt oppnåelige termodynamiske prosessen. I praksis er det mange faktorer som reduserer effektiviteten, for eksempel det faktum at isolasjon aldri er perfekt, og i adiabatiske stadier er det faktisk kaloriutveksling med utsiden.
I tilfelle av en bil blir motorblokken oppvarmet. På den annen side oppfører gass- og luftblandingen seg ikke nøyaktig som en ideell gass, som er utgangspunktet for Carnot -syklusen. Dette for å nevne bare noen faktorer som vil forårsake en drastisk ytelsesreduksjon.
Eksempler
Et stempel inne i en sylinder
Hvis systemet er et stempel låst i en sylinder som i figur 4, stiger stempelet under den isotermiske ekspansjonen, som det kan sees i det første skjemaet for det ekstreme venstre og også stiger under den adiabatiske ekspansjonen.
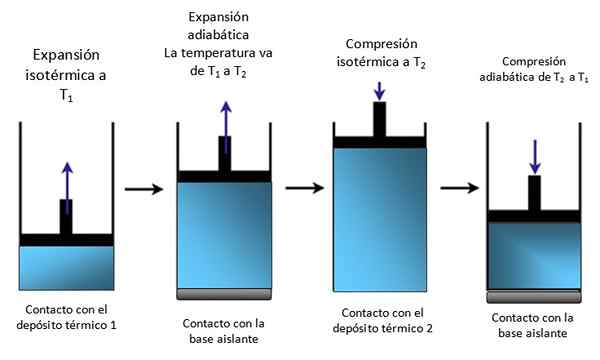 Figur 4. Bevegelse av et stempel inne i en sylinder. Kilde: Selvlaget.
Figur 4. Bevegelse av et stempel inne i en sylinder. Kilde: Selvlaget. Deretter komprimert isomisk, gir varme og fortsetter å komprimere adiabatisk. Resultatet er en bevegelse der stempelet stiger og ned i sylinderen og kan overføres til andre deler av en bestemt enhet, for eksempel en bilmotor, som produserer et par, eller en dampende maskin.
Forskjellige reversible prosesser
I tillegg til utvidelse og komprimering av en ideell gass inne i en sylinder, er det andre ideelle reversible prosesser som en Carnot -syklus kan konfigureres, for eksempel:
- Bevegelser av tur / retur i fravær av friksjon.
- En ideell vår som er komprimert og dekomprimert og som aldri er deformert.
- Elektriske kretsløp der det ikke er noen motstand som forsvinner energi.
- Magnetisering og demagnetiseringssykluser der det ikke er tap.
- Laster og laster ned et batteri.
Et atomkraftverk
Selv om det er et veldig komplekst system, er en første tilnærming til det som kreves for å produsere energi i atomreaktor den som følger:
- En termisk kilde, bestående av et materiale som går i oppløsning radioaktivt som uran.
Kan tjene deg: Gjeldende atommodell- Vasken eller den kalde termiske avsetningen som ville være atmosfæren.
- "Carnot -maskinen" som bruker en væske, nesten alltid rennende vann, som leveres varme fra den termiske kilden for å gjøre den til damp.
Når syklusen blir utført, oppnås strøm som nettverk. Når det blir transformert til damp med høy temperatur, blir vann nådd til en turbin, der energi blir omdannet til bevegelse eller kinetisk energi.
Turbinen aktiverer igjen en elektrisk generator som forvandler energien til bevegelsen til strøm. I tillegg til fiske materiale som uran, kan selvfølgelig fossilt brensel brukes som varmekilde.
Løste øvelser
-Eksempel 1: Effektivitet av en termisk maskin
Effektiviteten til en termisk maskin er definert som forholdet mellom utgangsarbeidet og inngangsarbeidet, og er derfor en dimensjonsløs mengde:
Maksimal effektivitet = (qinngang - Q exit) /Qinngang
Betegner maksimal effektivitet som eMaks, Det er mulig å demonstrere sin temperaturavhengighet, som er den enkleste variabelen å måle, for eksempel:
ogMaks = 1 - (t2/T1)
Hvor t2 Det er temperaturen på vasken og t1 Det er den termiske kildetemperaturen. Siden sistnevnte er større, viser effektiviteten seg alltid å være mindre enn 1.
Anta at en termisk maskin er i stand til å jobbe på følgende måter: a) mellom 200 K og 400 K, B) mellom 600 K og 400 K. Hva er effektiviteten i hvert tilfelle?
Løsning
a) I det første tilfellet er effektiviteten:
ogMax1 = 1 - (200/400) = 0.femti
b) For den andre modusen vil effektiviteten være:
ogMax2 = 1- (400/600) = 0.33
Selv om temperaturforskjellen er den samme mellom begge modusene, er ikke effektiviteten. Og enda mer bemerkelsesverdig er at den mest effektive modusen fungerer ved lavere temperatur.
-Eksempel 2: Absorbert varme og avgitt varme
En termisk maskin på 22 % produserer 1530 J arbeid. Finn: a) Mengden varme som er absorbert fra termisk avsetning 1, b) Mengden varme kassert til termisk tank 2.
a) I dette tilfellet brukes effektivitetsdefinisjonen, siden arbeidet som er gjort, ikke av temperaturene til de termiske avsetningene er tilgjengelig. 22% effektivitet betyr at E Maks = 0.22, derfor:
Maksimal effektivitet = arbeid /qinngang
Mengden varme som absorberes er nettopp Qinngang, Så rydding du har:
Qinngang = Arbeid/effektivitet = 1530 j/0.22 = 6954.5 J
b) Mengden varme som er tilordnet den kaldeste tanken er fra ΔW = qinngang - Qexit
Qexit = Qinngang - ΔW = 6954.5 -1530 J = 5424.5 J.
En annen måte er fra ogMaks = 1 - (t2/T1). Ettersom temperaturer ikke er kjent, men disse er relatert til varme, kan effektiviteten også uttrykkes som:
ogMaks = 1 - (qSceding/Qabsorbert)
Referanser
- Bauer, w. 2011. Fysikk for ingeniørfag og vitenskap. Volum 1. Mc Graw Hill. 654-657
- Kjernekraft. Drift av et atomkraftverk. Gjenopprettet fra: Energy-Nuclear.nett
- Serway, r., Jewett, J. (2008). Fysikk for vitenskap og ingeniørfag. Volum 1. 7. Ed. Cengage Learning. 618-622.
- Tippens, p. 2011. Fysikk: konsepter og applikasjoner. 7. utgave. MacGraw Hill. 414-416.
- Walker, J.2008. Fysikk. 4. utg.Addison Wesley. 610-630
- « Respekt på skolen hvordan du bruker det og konsekvenser
- Oppvarmingskurve hva som er, hvordan det er, eksempler »

